
Brennstoffzelle ist eine galvanische Zelle, die die chemische Reaktionsenergie eines kontinuierlich zugeführten Brennstoffes und eines Oxidationsmittels in elektrische Energie wandelt. Wenn auch mit Brennstoffzelle oft eine Wasserstoff-Sauerstoff-Brennstoffzelle gemeint ist, können je nach Brennstoffzellentyp außer Wasserstoff auch viele andere Brennstoffe genutzt werden, insbesondere Methanol, Butan oder Erdgas. Bennstoffzellen alleine sind keine Energiespeicher, sondern Energiewandler, denen Energie in chemisch gebundener Form mit den Brennstoffen zugeführt wird. Ein komplettes Brennstoffzellensystem kann aber einen Brennstoffspeicher enthalten. Die gemessen an der Zahl der installierten Geräte wichtigsten Anwendungen der Brennstoffzelle sind die netzunabhängige Stromversorgung sowie – vor allem in Japan – die Versorgung von Gebäuden mit Wärme und Elektrizität (Mikro-Kraft-Wärme-Kopplung). Dazu wurden bis zum April 2019 in Japan etwa 305.000 Gebäude mit Brennstoffzellenheizungen ausgestattet und diese staatlich bezuschusst („ENE-FARM“-Programm). In Deutschland wurden bis Januar 2019 knapp 5700 Anträge auf KfW-Förderung bewilligt. ie zahlenmäßig zweitwichtigste Anwendung der Brennstoffzelle ist die Versorgung netzferner Geräte wie Messstationen oder Elektrogeräte beim Camping. Für diesen Zweck verwendet man Direktmethanolbrennstoffzellen, von denen ein Hersteller bis Januar 2019 nach eigenen Angaben über 40.000 Geräte verkaufte. Drittens werden Fahrzeuge mit Brennstoffzellen betrieben, darunter mehr als 20.000 Gabelstapler, Hubwagen oder ähnliches, viele davon in den USA. Der Bestand an Brennstoffzellenfahrzeugen erhöhte sich 2018 um rund 4000 und lag am Ende bei etwa 11.200 Autos und Kleinlastwagen. Allein vom Toyota Mirai wurden bis September 2019 über 10.000 Fahrzeuge produziert. Außerdem waren bis September 2019 weltweit etwa 200 Brennstoffzellenbusse in Betrieb, etwa 70 in Europa, 40 in China, 18 in Japan und 71 in den USA.
Aufbau
Eine Brennstoffzelle besteht aus Elektroden, die durch einen Elektrolyten (Ionenleiter) voneinander getrennt sind. Der Elektrolyt kann aus einer semipermeablen Membran bestehen, die nur für eine Ionensorte, z. B. Protonen, durchlässig ist.
Die Elektrodenplatten/Bipolarplatten bestehen meist aus Metall oder Kohlenstoff, z. B. aus einem Kohlenstofffilz. Sie sind mit einem Katalysator beschichtet, zum Beispiel mit Platin oder mit Palladium. Der Elektrolyt kann flüssig (beispielsweise Laugen oder Säuren, Alkalicarbonatschmelzen) oder fest sein (etwa Keramiken oder Membranen).
Die Energie liefert eine Reaktion von Sauerstoff mit dem Brennstoff, der Wasserstoff sein kann, jedoch ebenso aus organischen Verbindungen wie beispielsweise Methan oder Methanol bestehen kann. Beide Reaktionspartner werden über die Elektroden kontinuierlich zugeführt.
Die theoretische Spannung einer Wasserstoff-Sauerstoff-Brennstoffzelle ist 1,23 V bei einer Temperatur von 25 °C. In der Praxis werden jedoch im Betrieb nur Spannungen von 0,5–1 V erreicht; nur im Ruhezustand oder bei kleinen Strömen werden Spannungen oberhalb 1 V erhalten. Die Spannung ist vom Brennstoff, von der Qualität der Zelle und von der Temperatur abhängig. Um eine höhere Spannung zu erhalten, werden mehrere Zellen zu einem Stack (engl. für ‚Stapel‘) in Reihe geschaltet. Unter Last bewirken die chemischen und elektrischen Prozesse ein Absinken der Spannung (nicht bei der Hochtemperatur-Schmelzkarbonatbrennstoffzelle, MCFC).
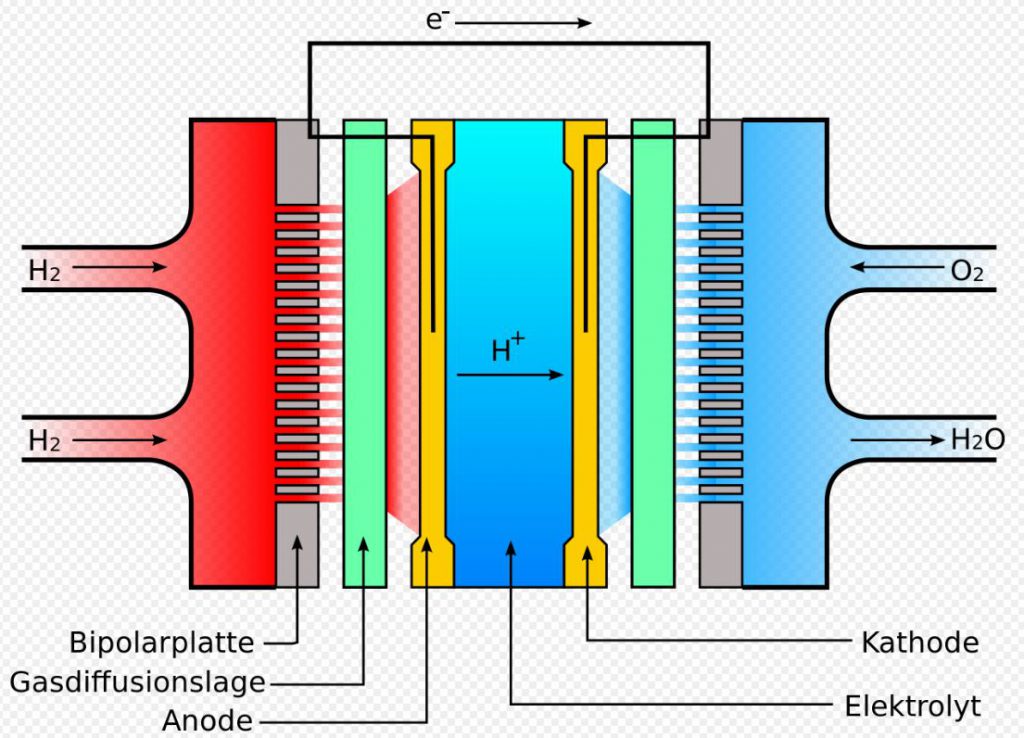
Bei der Niedertemperatur-Protonenaustauschmembran-Brennstoffzelle (Proton Exchange Membrane Fuel Cell, PEMFC; oder Polymer Electrolyte Fuel Cell, PEFC) ist der Aufbau wie folgt:
- Bipolarplatte als Elektrode mit eingefräster Gaskanalstruktur, beispielsweise aus leitfähigen Kunststoffen (durch Zugabe von zum Beispiel Carbon-Nanoröhrchen elektrisch leitend gemacht);
- poröse Carbon-Papiere;
- Reaktivschicht, meist auf die Ionomermembran aufgebracht. Hier stehen die vier Phasen Katalysator (Pt), Elektronenleiter (Ruß oder Carbon-Nanomaterialien), Protonenleiter (Ionomer) und Porosität miteinander in Kontakt;
- protonenleitende Ionomermembran: gasdicht und nicht elektronenleitend.
Chemische Reaktion
Die Gesamtreaktion einer Brennstoffzelle entspricht der Verbrennungsreaktion des Brennstoffes. Daher nennt man die Umsetzung in einer Brennstoffzelle auch „kalte Verbrennung“, wobei direkt (d. h. ohne Umweg über Wärmeenergie) elektrische Energie erhalten wird.
Wasserstoff-Sauerstoff-Brennstoffzelle
Das Prinzip der Brennstoffzelle basiert auf der nachfolgenden Reaktionsgleichung:

Viele Brennstoffzellentypen können diese Reaktion zur Gewinnung elektrischer Energie nutzen. Der heute für viele Anwendungen wichtigste Brennstoffzellentyp dafür ist die Protonenaustauschmembran-Brennstoffzelle (PEMFC). Eine solche Brennstoffzelle verwendet in der Regel Wasserstoff (der mittels Dampfreformierung aus Methanol oder Methan erzeugt werden kann) als Energieträger und erreicht einen Wirkungsgrad von etwa 60 %. Das Kernstück der PEMFC ist eine Polymermembran, die ausschließlich für Protonen durchlässig ist (also nur für H+-Ionen), die so genannte proton exchange membrane (PEM). Das Oxidationsmittel, für gewöhnlich Luftsauerstoff, ist dadurch räumlich vom Reduktionsmittel getrennt.
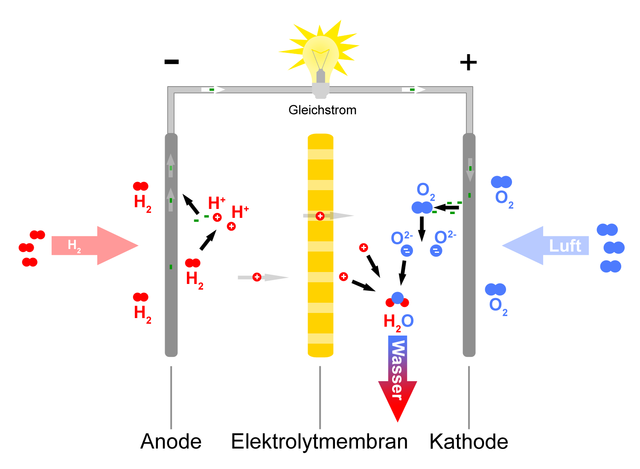
Der Brennstoff, hier Wasserstoff, wird an der Anode katalytisch unter Abgabe von Elektronen zu Protonen oxidiert. Diese gelangen durch die Ionen-Austausch-Membran in die Kammer mit dem Oxidationsmittel. Die Elektronen werden aus der Brennstoffzelle abgeleitet und fließen über einen elektrischen Verbraucher, zum Beispiel eine Glühlampe, zur Kathode. An der Kathode wird das Oxidationsmittel, hier Sauerstoff, durch Aufnahme der Elektronen zu Anionen reduziert, die unmittelbar mit den Wasserstoffionen zu Wasser reagieren.
Brennstoffzellen mit einem solchen Aufbau heißen Polyelektrolyt-Brennstoffzellen, PEFC (für Polymer Electrolyte Fuel Cell) oder auch Protonenaustauschmembran-Brennstoffzelle, PEMFC (für Proton Exchange Membrane Fuel Cell). Die verwendeten Membranen sind saure Elektrolyten.
Redox-Reaktionsgleichungen für eine PEMFC:

Anwendungsbereich Straßenverkehr:
Mit Stand Juli 2019 waren allein in den USA über 7.000 Brennstoffzellenautos verkauft worden, während der Bestand an Brennstoffzellenfahrzeugen in Japan zu diesem Zeitpunkt bei über 3.200 Autos lag.[9] In Deutschland waren im Juni 2019 nur 386 Brennstoffzellenautos zugelassen.[45]

Neben dem Toyota Mirai mit über 7.000 verkauften Exemplaren bis zum März 2019 vertrieb allein Hyundai im europäischen Markt über 500 Hyundai ix35 FCEV sowie insgesamt über 600 Hyundai Nexo.

Im Jahr 2017 wurden weltweit über 3.300 Personenkraftwagen mit Wasserstoff-Brennstoffzellenantrieb verkauft: über 2.600 Toyota Mirai, über 500 Honda Clarity FCEV und knapp 200 Hyundai ix35/Tucson FCEV. 2018 wurden in den USA über 2.300 Wasserstoffautos verkauft, darunter 1700 Toyota Mirai und über 600 Honda Clarity Fuel Cell.
Ein Auslöser für erheblichen Anstrengungen zur Forschung und Entwicklung der Brennstoffzellen war der Zero emission act bzw. das Zero Emission Vehicle mandate (ZEV) in den USA, die vorsahen, dass Autos zukünftig abgasfrei fahren sollen. Für das Jahr 2003 war vorgesehen, dass 10 % aller neu zugelassenen Fahrzeuge in Kalifornien diesem Gesetz unterliegen sollten. Kurz vorher, nach massivem Druck der amerikanischen Automobilindustrie, wurde das ZEV jedoch gekippt, obgleich es weiterhin diskutiert wird.
Durch den verstärkten Einsatz von emissionsfreien Fahrzeugen in Ballungszentren und Großstädten wird eine Verbesserung der dortigen Luftqualität erwartet. Ein Nebeneffekt wäre allerdings, dass die Emissionen vom Ort der Fahrzeugnutzung dorthin verlagert werden, wo der Wasserstoff hergestellt wird, soweit das nicht aufgrund klimaneutraler Verfahren erfolgt. Für die Wasserstoffherstellung gibt es mehrere Möglichkeiten mit unterschiedlicher Effizienz.
Für den breiten Einsatz der mobilen Wasserstoffanwendungen ist der gleichzeitige Aufbau von Wasserstofftankstellen erforderlich; davon waren Ende 2018 weltweit 376 in Betrieb. Für die Mitnahme von Wasserstoff in Fahrzeugen werden heute praktisch nur noch Druckbehälter verwendet. Auch Formen der Wasserstoffspeicherung sind möglich, beispielsweise in Metallhydriden oder bei niedriger Temperatur als flüssiger Wasserstoff. Bei der Gesamtbeurteilung des Energieeffizienz ist dabei der hohe Energiebedarf für die Komprimierung (bis 700 bar) oder die Verflüssigung (etwa −250 °C) zu beachten, der den Gesamtwirkungsgrad (Well-to-Wheel) der Fahrzeuge mit Wasserstoffspeichern deutlich senkt.
Trotz des hohen Wirkungsgrads der Brennstoffzelle gestaltet sich auch die Abfuhr der Abwärme auf dem vergleichsweise niedrigen Temperaturniveau der PEM-Brennstoffzelle von etwa 80 °C als problematisch, denn im Gegensatz zum Verbrennungsmotor beinhaltet das relativ kalte Abgas (Wasserdampf) nur eine vergleichsweise geringe Wärmemenge. Demzufolge ist man bestrebt, die Betriebstemperatur der PEM-Brennstoffzelle auf über 100 °C anzuheben, um leistungsstärkere Brennstoffzellen-Automobile mit mehr als 100 kW realisieren zu können.
Bei Temperaturen unterhalb des Gefrierpunkts könnte die Startfähigkeit der Brennstoffzelle aufgrund gefrierenden Wassers beeinträchtigt sein. Es muss sichergestellt sein, dass die elektrochemische Reaktion, insbesondere die Diffusion der Brenngase, nicht durch Eisbildung behindert wird. Das kann beispielsweise durch eine geeignete Elektrodenstruktur erzielt werden. In der Praxis sind weder Kälte noch Hitze ein Problem für Brennstoffzellenautos.
Quelle: Wikipedia
Brennstoffzelle im Auto: Besser als Lithiumakkus? | Harald Lesch